Водородная связь: механизм образования ее между молекулами, примеры
Ключевые слова конспекта: Водородная химическая связь: меж- и внутримолекулярная. Значение водородной связи в природе и жизни человека.
Молекулы электронейтральны, однако и между ними могут возникнуть силы взаимного притяжения, получившие название вандервальсова взаимодействия в честь голландского учёного, лауреата Нобелевской премии Йоханнеса Дидерика Ван-дер-Ваальса. Причиной такого притяжения является электромагнитное взаимодействие электронов и ядер одной молекулы с электронами и ядрами другой. Межмолекулярные связи значительно менее прочные, чем химические. Однако именно они приводят к тому, что вещества молекулярного строения могут существовать в конденсированном, т. е. жидком или твёрдом, состоянии.
Силы Ван-дер-Ваальса — предмет изучения физики. Однако к межмолекулярному взаимодействию относят и водородную связь, которая имеет большое значение в химии и биологии.
Энергия водородной связи составляет всего лишь 4—40 кДж/моль, т. е. соответствует энергетической характеристике межмолекулярных сил. Поэтому её можно рассматривать как частный случай вандерваальсовых сил взаимодействия. Несмотря на низкие энергетические характеристики, а может быть именно благодаря им, водородная связь — основа организации и функционирования живой материи на нашей планете.
| Водородная связь образуется между атомом водорода, связанным ковалентной связью с электроотрицательным атомом одной молекулы и атомами фтора, кислорода, азота другой молекулы, имеющими неподелённые электронные пары. |
Это определение справедливо для межмолекулярной водородной связи.

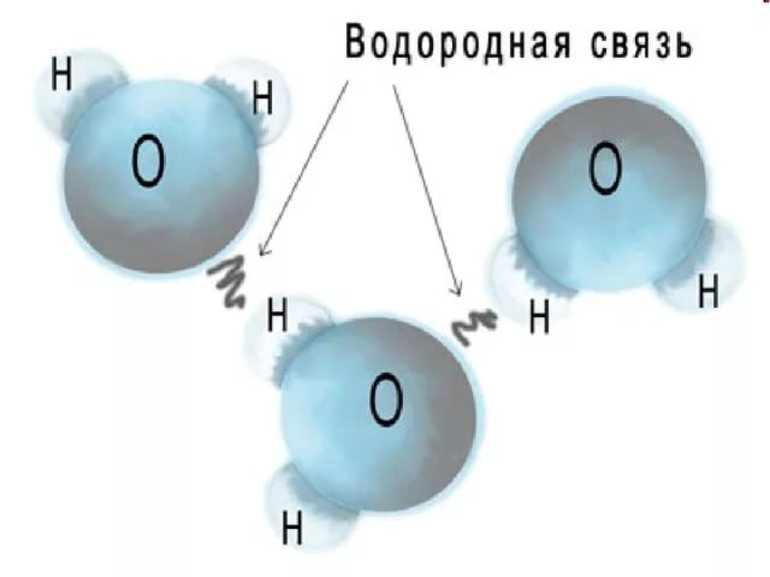
Рассмотрим образование водородной связи на примере воды. Как вы уже знаете, молекула воды имеет угловое строение. Помимо двух общих с атомами водорода электронных пар, атом кислорода имеет две неподелённые электронные пары. Кислород, как атом более электроотрицательного элемента, обладает частичным отрицательным зарядом δ – . Атомы водорода несут частичный положительный заряд δ + . Вполне естественно, что между атомом водорода одной молекулы и неподелённой электронной парой атома кислорода другой молекулы возникает электростатическое притяжение (водородную связь обозначают троеточием):
В молекуле воды — два атома водорода и две неподелённые электронные пары. Следовательно, каждая молекула способна к образованию не одной, а четырёх водородных связей. Образуется своеобразный пространственный каркас, скрепляющий между собой множество молекул воды.
Водородная связь может возникать между атомами водорода и атомами неметаллов с высокой электроотрицательностью (фтора, кислорода, азота), обладающих неподелёнными парами электронов.
Водородная связь примерно в 10 раз слабее, чем ковалентная полярная, однако она сцепляет молекулы воды друг с другом. В результате вода приобретает аномальные свойства, которые позволяют считать её самым удивительным веществом на Земле.
Например, для того чтобы оторвать одну молекулу воды от другой, требуется затратить некоторое количество энергии. Если бы водородных связей не было, вода закипала бы при температуре –80 °С, а замерзала бы при –100 °С. В таком случае наша Земля превратилась бы в безжизненную пустыню: все реки, моря и океаны выкипели бы, а на небе не было бы ни облачка, ни тучки.
Плотность воды тоже аномальна. В твёрдом агрегатном состоянии (лёд) молекулы воды «упакованы» так, что между ними остаётся много «пустого места». Поэтому плотность льда меньше, чем плотность воды, и лёд плавает на её поверхности. Благодаря этому аномальному свойству даже при самых сильных морозах температура воды на глубине подо льдом не опускается ниже +4 °С. Именно при такой температуре плотность воды самая большая, а потому лёд легче воды и в ней не тонет. Это позволяет глубоким водоёмам не промерзать зимой до дна, что спасает жизнь водным обитателям.
Удивительная красота и многообразие снежинок — также результат работы водородных связей.

Благодаря водородным связям вещества с низкими относительными молекулярными массами ассоциированы в жидкости, например, первые члены гомологических рядов предельных одноатомных спиртов и карбоновых кислот. Эти вещества, как и некоторые многоатомные спирты (этиленгликоль, глицерин), благодаря водородным связям неограниченно растворимы в воде:

Водородная связь способствует лёгкому переходу некоторых веществ (например, аммиака, фтороводорода) из газообразного состояния в жидкое и обратно:
Это свойство аммиака позволяет использовать его в качестве хладагента в промышленных холодильных установках.
Рассмотрим ещё одну разновидность водородной связи, которая играет большую роль в организации структур таких важнейших биополимеров, как белки и нуклеиновые кислоты. Так как эта связь возникает внутри полимерных молекул, она называется внутримолекулярная водородная связь. Именно эта связь определяет вторичную структуру белка и двойную спираль ДНК.


Разрушение вторичной структуры белка приводит к его денатурации.
Каждая половинка двойной спирали представляет собой полимер, построенный из четырёх видов нуклеотидов, — полинуклеотид. Строгий порядок расположения остатков нуклеотидов одной цепи ДНК напротив нуклеотидов другой формируется именно за счёт водородных связей по принципу комплементарности: между остатками аденинового (А) и тиминового (Т) нуклеотидов — две водородные связи, между цитозиновым (Ц) и гуаниновым (Г) — три водородные связи.
Водородные связи играют важную роль в процессе передачи наследственной информации. При самоудвоении ДНК водородные связи материнской молекулы разрываются и синтезируются две новые цепи полинуклеотидов, в соответствии с принципом комлементарности. В итоге возникают две новые молекулы ДНК, в каждой из которых одна цепь была взята из материнской ДНК, а вторая, комплементарная ей, была выстроена заново.
Водородные связи — основа соблюдения строгой программы синтеза мРНК и затем соответствующего белка. Следовательно, без водородных связей невозможно было бы существование белковых организмов на нашей планете.
За открытие структуры двойной спирали дезоксирибонуклеиновой кислоты (ДНК) американские биологи Джеймс Уотсон и Фрэнсис Крик были удостоены Нобелевской премии.
Конспект урока по химии «Водородная химическая связь». В учебных целях использованы цитаты из пособия «Химия. 11 класс : учеб, для общеобразоват. организаций : базовый уровень / О. С. Габриелян, И. Г. Остроумов, С. А. Сладков. — М. : Просвещение». Выберите дальнейшее действие:
Водородная связь
Водородная связь весьма распространена и играет важную роль в биологических объектах. Рассмотрим ее образование подробнее.
Образование водородной связи
При возникновении подходящих условий водородная связь возникает самопроизвольно.
Какие же условия приводят к возникновению водородной связи?
Можно предположить, что в любом ряду веществ с молекулами одинаковой формы и полярности температуры плавления и кипения должны повышаться прямо пропорционально возрастанию молекулярной массы, однако существуют некоторые несоответствия.
На следующем рисунке приведены кривые зависимости температуры кипения гидридов элементов 6 группы от молекулярной массы.

зависимость температуры кипения и температуры плавления от молекулярной массы соединений
Так, для гидридов элементов 6 группы наблюдается последовательное увеличение температур кипения и плавления с увеличением молекулярной массы (номера периода), но из этой закономерности выпадает вода.
В 5 группе аномально высокие температуры кипения и плавления наблюдаются у аммиака NH3, а в 7 группе – у HF, по сравнению с гидридами элементов соответствующих групп.
Почему вода, аммиак и фтороводород имеют аномально высокие температуры кипения и плавления?
Это связано с присутствием в воде, аммиаке и фтороводороде водородных связей.
Водородная связь — это внутри- или межмолекулярная связь, которая образуется с соединениях между атомами водорода и атомами, имеющими большую электроотрицательность (N, O, F).
Механизм образования водородной связи, вследствие электростатического притяжения атомов — электростатический. Но частично он также носит донорно–акцепторный характер.
Образуемые соединения имеют большую полярность, возникает диполь. Атом водорода находится на положительном конце диполя. Этот диполь может взаимодействовать с неподеленной электронной парой кислорода (и азота, и фтора), который принадлежит другой или этой же молекуле. Таким образом, донором электронной пары являются атомы F, O или N, а акцептором — атомы водорода.
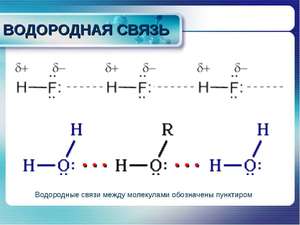
Графически, на рисунках, водородная связь обозначается тремя точками:

Виды водородной связи
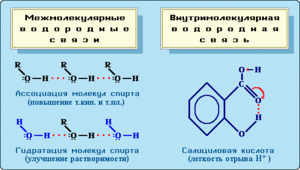
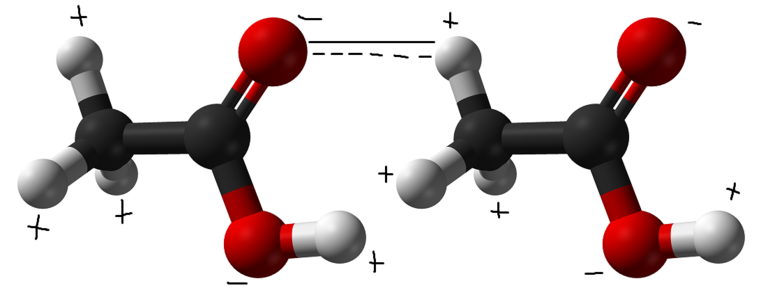
- Межмолекулярная водородная связь образуется между различными молекулами веществ. Обязательным условием образования такого вида водородной связи — это наличие водорода в одной молекуле и одного из элементов с высокой электроотрицательностью в другой молекуле (например, F, O, N, Cl, S). Связь может возникать как между одинаковыми молекулами, так и между разными. Например, это могут быть молекулы аммиака, воды, фтороводорода, спиртов (например, метанол, этанол), карбоновых кислот (например, муравьиная, уксусная кислоты), аминокислот в молекуле белка:

- Внутримолекулярная водородная связь образуется внутри одной молекулы. Условие образования внутримолекулярной водородной связи — это наличие в одной молекуле и атомов водорода и атомы с высокой электроотрицательностью. Такая связь может возникнуть, например, у многоатомных спиртов (этиленгликоль, глицерин), белков, углеводов, оксикислот (салициловая кислота) и других органических соединений:

Характеристика водородной связи
Водородная связь характеризуется
- Направленностью в пространстве и насыщаемостью.
- Водородная связь оказывает большое влияние на свойства многих веществ, особенно в биологических системах. Например, водородная связь определяет довольно некомпактную упаковку молекул воды во льду, поэтому плотность льда меньше плотности жидкой воды. Наличие водородной связи в веществах способствует аномальному росту их температур кипения и плавления.
- Водородная связь — слабая связь. Величина энергии водородной связи обычно лежит в пределах от 4 до 25 кДж/моль, это всего несколько процентов от величины энергии обычной химической связи. Теперь предположим, что водородная связь возникает в результате электростатического взаимодействия между диполем связи X-H и неподеленной электронной порой на атоме Y. Тогда прочность водородной связи увеличивается в ряду:
N-H···Y ˂ O-H···Y ˂ F-H···Y
Т.е., связь тем прочнее, чем меньше размер атома с неподеленными парами — N, O, F и больше его электроотрицательность. Среди них более прочную водородную связь образует тот, неподеленная электронная пара которого менее сильно притягивается к своему ядру.
Механизм образования водородной связи
Гидрогенная связь — образовывается между «+» заряженными атомами водорода и «-» заряженными атомами других молекул.
Очень часто эта взаимосвязь возникает и существует из-за взаимодействия атома водорода с такими атомами: оксиген (О), нитроген (N). Это происходит вследствие того, что данные элементы имеют небольшой удельный вес и характеризуются высокой электроотрицательностью. Элементы, которые имеют больший удельный вес — сера S или хлор Cl—связываются с водородом менее прочно, хотя их электроотрицательность сравнима с нитрогеном.
Типы гидрогенной связи
- Межмолекулярная водородная — возникает между двумя элементами, пример: метиловый спирт.
- Водородная (гидрогенная) внутримолекулярная — образуется внутри элемента, пример: 2-нитрофенол.
Межмолекулярная гидрогенная связь

Совместная электронная пара смещается от атома водорода к отрицательно заряженному атому. При этом водород входит в комплекс с неразделенной электронной парой другого атома или иона.
Н-связь графически изображают в виде точек, тем самым показывая, что она слабее ковалентной (примерно в 10−15 раз).
Молекулы воды (две) и молекулы уксусной кислоты (две)
Внутримолекулярная гидрогенная взаимосвязь. Ей свойственно находиться в таких структурах, как многоатомные спирты, углеводы, белки.
Молекула салициловой кислоты
Химические взаимодействия делятся на слабые и сильные. Их отличие состоит в том, что при разрыве они выделяют разную энергию и у них различные по длине (расстояние между атомами):
1. Слабые. Содержание энергии — 15−25 кдж/моль, длина равна 30.
2. Сильные. Энергия — 300 кдж/моль, длина 22−23.
Для образования Н-св. характерно два типа отдачи ионов — электростатический и донорно — акцепторный. Интересно то, что донором выступает более сильный элемент (F, O, N), а акцептором — атом водорода.
Механизм образования водородной связи
Хорошо разбирать механизм образования водородной связи на примере её между молекулами воды. Н-св. на рисунках обозначается 3 точками. Атом гидрогена имеет всего лишь один электрон, который при взаимодействии с атомом большей электроотрицательности может условно оголять ядро, что, в свою очередь, образует дополнительную взаимосвязь с другим атомом. Это и есть водородная связь.
Вода — это вещество, между молекулами которого образуются водородные связи.
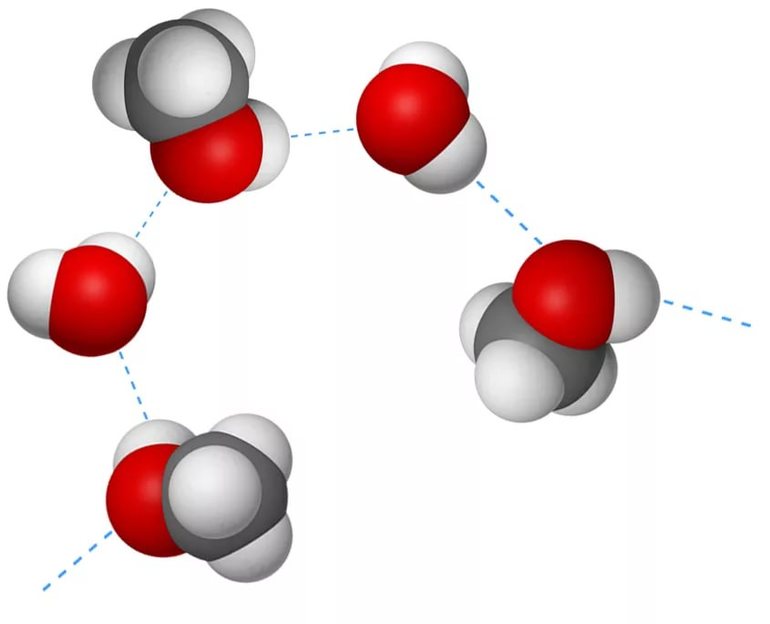
Кластеры из нескольких молекул воды
Благодаря водородным взаимосвязям молекулы воды взаимодействуют друг с другом, что приводит к образованию кластеров или комплексов воды. Одним из ярких примеров является димер воды.
Н-св. считаются довольно слабыми и неустойчивыми: считается, что они легко возникают, но и также легко разрушаются. Для водородных связей характерен симптом тепловой флюктуации. Вода представляет собой сеть из молекул, связанных водородными связями.
Аномальные свойства, обеспеченные водородной взаимосвязью
Молекула воды состоит из трёх молекул и содержит 4 Н-св. Здесь присутствуют 2 атома водорода , а кислород, имея две неподеленные электронные пары, связывается с атомами Н ближайших молекул Н2О.
Н-св. обеспечивают высокие температуры кипения и плавления. Без них эти показатели были бы намного меньше.
Н-св. в молекулах воды обладают достаточной силой и препятствуют её плавлению и испарению.
А также они обеспечивают ещё одно свойство Н2О, которое характеризуется тем, что при плавлении воды её плотность повышается.
Наибольшее значение имеет плотность воды (1,00 г/мл) при температуре 4 градуса Цельсия. Эта температура характерна для зимнего времени и находится на дне пресных водоёмов, там же и находится вода с максимальной плотностью.
Как изменяются свойства веществ в зависимости от водородной связи
Наиболее достоверным признаком наличия в веществе межмолекулярной Н-св. является показатель кипения вещества. Одна из высоких температур кипения у воды (100 o C так как для того чтобы разрушить межмолекулярные связи в H2O нужно затратить больше энергии). Н-св. сильно может влиять на физические и химические свойства вещества. Межмолекулярная связь обеспечивает повышение температуры плавления и кипения различных веществ. Вещества, которые содержат ОН-группы —моносахариды, дисахариды, как правило, обладают отличной гидрофильностью.
Водородная связь

Водородная связь – уникальный тип химического взаимодействия между молекулами одного вещества. Часто термин “водородная связь” обозначается в тексте как “Н-связь”. Н – связь образуется самостоятельно при подходящих условиях и выражается в межмолекулярных и внутримолекулярных взаимодействиях. В образовании водородной связи участвует положительно поляризованный атом водорода, связывающий между собой атомы элементов с высокой электроотрицательностью. Данный тип связи не образуется, если электроотрицательность водорода и элемента, взаимодействующего с ним, близка по значению. В основном водородная связь возникает при участии кислорода, фтора и азота, потому что атомы этих элементов обладают высоким значением электроотрицательности и малыми размерами. Если же у атомов значение электроотрицательности и размер высоки, например, как у хлора или серы, то образовавшаяся водородная связь будет очень слабой. Обычно водородную связь обозначают тремя точками.
Механизм образования водородной связи
Образование водородной связи происходит частично по электростатическому, частично по донорно-акцепторному механизму. Донором является электроотрицательный элемент, а акцептором непосредственно водород. Отследить механизм образования водородной связи можно на простом примере молекулы воды. Так как ковалентная связь О-Н является сильно полярной, то на атоме кислорода образуется частично отрицательный заряд, соответственно на атоме водорода – частично положительный. В связи с этим электрон водорода подвергается сильному смещению, его орбиталь освобождается, и свободная электронная пара кислорода другой молекулы воды начинает взаимодействовать с ней. Это и есть водородная связь, при которой между двумя электроотрицательными атомами кислорода находится один атом водорода. С одним из атомов кислорода он связан ковалентной связью, с другим – водородной.
Типы водородной связи
Существует два типа водородной связи:
Межмолекулярная – возникает между положительно поляризованным атомом водорода одной молекулы и отрицательно поляризованным атомом неметалла другой молекулы. Образование этого типа связи сопровождается кардинальными изменениями в свойствах веществ: вязкость, диэлектрическая постоянная, температуры плавления и кипения повышаются. Примерами данного типа водородной связи являются различные карбоновые кислоты, а также аммиак, метанол и фтороводород.Также одним из ярчайших примеров межмолекулярной водородной связи является вода.
Внутримолекулярная – возникает при условии, что положительно поляризованный атом водорода связывается с другим, но отрицательно заряженным атомом одной и той же молекулы. Вещества с этим типом связи обладают сравнительно низкой вязкостью, температурами плавления и кипения, а также наиболее летучи. Ярким примером такого типа связи являются салициловая кислота, молекулы белков, а также молекула ДНК.
Примеры соединений с водородной связью
Помимо уже известного нам яркого представителя веществ с водородной связью – воды, существует множество других примеров. Данный тип связи играет значительную роль в существовании различных органических веществ, белков. а также некоторых полимеров. Из-за малой прочности, водородные связи имеют свойство легко появляться и также легко исчезать при нормальной температуре. Это свойство оказывает большое влияние на различные биологические процессы. Так, имеется предположение, что наследственность напрямую зависит от водородной связи: действие памяти связывают с хранением информации в молекулярных конфигурациях, соединённых с помощью данного типа связи. Цепи ДНК являются ярчайшим примером соединений с водородной связью. Также молекулы спиртов соединены между собой с помощью водородной связи, благодаря которой они обладают высокой температурой плавления и кипения.
Еще по этой теме:

Серная кислота
Основные сведения о серной кислоте: свойства, получение, применение.

Теперь «ХиШник» стал полностью бесплатным
Как развивалось приложение все эти годы, и почему мы им так гордимся.
Азотная кислота
Статья содержит основную информацию об азотной кислоте: её свойства, получение и применение.

Диены
Основные сведения о диеновых углеводородах: номенклатура и изомерия, классификация, химические свойства, получение.
Правило Марковникова
Правило Марковникова: формулировка, механизм протекания реакций, исключения из правила.

Таблицы для ЕГЭ по химии
В статье представлены таблицы, необходимые при изучении химии и сдаче ЕГЭ.

Внеклассное мероприятие по химии
Идеи интересных внеклассных мероприятий по химии.

Формулы для решения задач по химии
Перечень основных формул, которые используются при решении школьных задач по химии.

Химические профессии
Обзор необычных профессий, связанных с химией.

ЕГЭ по химии 2019
Основная информация о ЕГЭ по химии 2019: структура экзамена, баллы, даты проведения.

Критерии оценивания ОГЭ по химии, баллы 2019
Подробно расскажем о баллах ОГЭ по химии 2019, методах и критериях оценивания заданий и переводе первичных баллов в школьную оценку.

Изменения ОГЭ по химии в 2019 году
Расскажем об изменениях, которые ждут школьников при сдаче ОГЭ по химии в 2019 году.

Подготовка к ОГЭ по химии
Несколько советов и рекомендаций, следуя которым подготовка к ОГЭ по химии будет проходить результативно.

Онлайн тесты по химии
Немного информации о проверке знаний с помощью тестов по химии в режиме онлайн.

Все об ОГЭ по химии в 2019
Основные сведения об ОГЭ по химии 2019: даты, время, баллы, материалы для подготовки.
Тест по химии 11 класс
Рассказываем о тестах по химии, используемых для проверки знаний в 11 классе.

Тест по химии 10 класс
Общие сведения о тестах по химии в 10 классе.
Тест по химии 9 класс
Рассказываем о тестах по химии, используемых для проверки знаний в 9 классе.
Тест по химии 8 класс
Рассказываем в общих чертах о тестах по химии в 8 классе
Ионная связь
Статья, содержащая в себе базовые понятие об ионном виде химической связи.
Подготовка к ЕГЭ по химии с нуля
В статье дано несколько действенных советов по подготовке к ЕГЭ по химии «с нуля».
Металлическая связь
Продолжаем серию статей про виды химической связи.
Ковалентная связь
Начинаем серию статей про виды химической связи.

Шкала перевода баллов ЕГЭ по химии 2018
Отвечаем на вопросы о системе оценивания и переводе первичных баллов в тестовые.
Учимся на летних каникулах
Размышляем о том, как полезно провести время во время летнего отдыха на каникулах. (в статье есть подарок внимательным читателям)
«ХиШник» приехал на Сахалин!
Этим летом открывается очередная летняя сессия областной профильной школы для одаренных детей «Эврика».

Мой сын увлёкся химией, что делать?
Собрали ТОП-5 полезных материалов для старшеклассника.
Двенадцать сервисов для изучения химии, с которыми ты точно сдашь
Великолепная подборка полезных сайтов для самостоятельного изучения химии.
О правах и обязанностях в школе: почему необходимо сотрудничество учеников и учителей
Что такое право само по себе и откуда оно берется. Как не заработать славу скандалистов, «вечно качающих права», и при этом не переносить безропотно нарушение своих личных границ…
Современный задачник по химии
материал о том, какие виды задачников по химии существуют и как среди них ориентироваться.
Выбираем репетитора по химии: инструкция
Или не выбираем
Научиться решать задачи по химии легко: следуем инструкции
Учимся решать задачи по химии к ОГЭ, ЕГЭ, инструкция от ХиШника
Изменения в ЕГЭ по химии 2018 года, новая демоверсия, спецификация, кодификаторы ЕГЭ
ФИПИ снова решил усложнить нам жизнь новыми требованиями к ЕГЭ. О том, почему изменения не всегда плохи, и как встретить их с достоинством.
Обновление в демонстрационной версии «ХиШника»
Мы расширили приветственное окно, чтобы при входе в приложение всем новым пользователям были понятны основные принципы работы «ХиШника».

Активация лицензионного ключа и первые шаги в «ХиШнике».
Что такое лицензионный ключ и как происходит его активация в приложении

Современный урок химии по ФГОС
Для чего нужны стандарты, по которым происходит обучение химии в российских школах, и как приложение “ХиШник” поможет соответствовать этим стандартам?

ХиШник в школе: ИКТ на уроках химии
Как наше приложение поможет внедрить ИКТ в уроки
Ура! Новые планы ХиШника и подарочки
Подводим итоги 2017, планируем 2018 и, конечно же, дарим подарки!
Родина приложения «ХиШник» – Новосибирский Академгородок
Почему же родиной «ХиШника» стал Новосибирский Академгородок?
Совпадение не случайное.
Можно ли просматривать историю решения задач учениками в онлайн-режиме?
Итак, «ХиШник» это приложение, в котором могут работать и ученики, и преподаватели. После того, как преподаватель создает в приложении учебную группу
Можно ли заниматься в «ХиШнике» со смартфона/планшета?
Сегодня у нас вопрос, которого мы давно ждали: можно ли заниматься в «ХиШнике» со смартфона/планшета?
Семинар от «ХиШника» на КПК для учителей химии
На прошлой неделе мы провели семинар в рамках масштабных ежегодных курсов повышения квалификации на базе СУНЦ НГУ (Новосибирск, Академгородок).
Команда «ХиШника» провела мастер-класс для преподавателей химии и методистов
Вчера команда «ХиШника» провела мастер-класс для преподавателей химии и методистов программ повышения квалификации из разных регионов России.
Как купить полный доступ к приложению?
Сегодня новый вопрос: что делать, если решать задачи в демо-версии приложения понравилось, как получить полный доступ? Отвечаем!

«ХиШник» представляет два кейса на ярмарке кейсов «Школа реальных дел»
Ярмарка кейсов «Школы реальных дел» – уже в эту пятницу! В этом году «ХиШник» представляет два кейса.
Служба поддержки:
support@hishnik-school.ru
Для СМИ:
onp@alekta.ru
Спасибо!
от 01.01.2017 года
Настоящее пользовательское (лицензионное) соглашение (далее – “Соглашение”) заключается между Обществом с ограниченной ответственностью “АЛЕКТА” (далее – “Лицензиар”), и Пользователем (физическим лицом, выступающем в роли конечного потребителя Продукта) совместно именуемые “Стороны”.
Пожалуйста, внимательно ознакомьтесь с текстом настоящего Соглашения. Оно представляет собой публичную оферту и, после его принятия Вами, образует соглашение между Вами (Пользователем) и Лицензиаром о предмете и на условиях, изложенных в тексте Соглашения.
Принимая настоящее Соглашение, Вы соглашаетесь с положениями, принципами, а также соответствующими условиями лицензионного соглашения, изложенными ниже.
Водородная связь в химии – как и где образуется, свойства, примеры
Водородная связь встречается во всех областях химии и проявляется в виде межмолекулярного или внутримолекулярного взаимодействия особых групп, одна из которых обязательно содержит реакционно-способный атом водорода с положительным зарядом. Это глобальное явление, называемое также H-связью, отличается от других объединений химических частиц тем, что образуется самопроизвольно в подходящих условиях, а не в результате направленного воздействия.
- Характерные особенности
- Проявление в неорганической химии
- Понятие водных кластеров
- Значение для органических соединений
Характерные особенности
Этот тип связи возникает в молекулах, когда их атом водорода, поляризованный положительно, взаимодействует с атомом другой молекулы, имеющим заряд отрицательный. Расстояние между атомами-участниками процесса должно оказаться меньше, чем сумма их радиусов. Выделяют два вида H-связей:
- Межмолекулярная. Возникает между различными молекулами веществ: для этого необходимо присутствие водорода и одного из элементов с хорошей способностью притягивать электроны других атомов. Высокая электроотрицательность фтора (F), кислорода (O), азота (N), хлора (Cl) и серы (S) служит этому надёжной поддержкой. Общие пары взаимодействующих электронов смещаются к атомам отрицательно заряженных элементов, а положительные электрические заряды водорода концентрируются в малых объёмах. Протоны взаимодействуют с электронными парами соседних атомов, что приводит к их обобществлению.
- Внутримолекулярная. Образуется в пределах одной молекулы, для чего в ней наряду с положительно заряженными атомами водорода должны присутствовать отрицательно поляризованные группы. Явление обнаруживается в природе у многоатомных спиртов, белков, углеводов и ряда других органических соединений.
Энергия H-связи обладает низкими прочностными характеристиками: она в несколько раз ниже, чем у остальных подобных взаимодействий. Это позволяет ей существовать промежуточным звеном между основными химическими связями (ковалентной, ионной и металлической) и силами притяжения и отталкивания Ван-дер-Ваальса, стремящимися удержать частицы в твёрдом или жидком состоянии. Кристаллические решётки с молекулами в узлах — характерная особенность веществ с водородной связью. Примеры можно привести различные:

- вода H2O в виде льда;
- кристаллы йода I;
- хлор Cl;
- бром Br;
- диоксид углерода CO2 в форме «сухого льда»;
- твёрдый аммиак NH3;
- конденсированная органика (метан CH4, бензол C6H6, фенол C6H5OH, нафталин C10H8, различные белки).
Механизм образования водородной связи считается смешанным — одновременно электростатическим и донорно-акцепторным. Решающая роль в этом принадлежит повышению электроотрицательности одного атома (A), позволяющей оттягивать в свою сторону электронную пару другого атома (H), принимающего участие в этом взаимодействии. В результате:
- первый атом приобретает частично отрицательный заряд (d-);
- второй участник заряжается положительно (d+);
- происходит поляризация химической связи (Аd-) — (Hd+).
Образовавшиеся атомы водорода, заряд которых частично положителен, обладают способностями притягивать другие молекулы, содержащие электроотрицательные группы. Эти электростатические взаимодействия и обуславливают появление Н-связей, для формирования которых необходимы три обязательных элемента:
- атом-донор протона;
- атом-акцептор протона;
- атом водорода Н.
Такое донорство в обычных условиях никогда не осуществляется на все 100%. Атом-донор остается химически связанным с водородом. Графически это обозначается в виде линии из точек, указывающей, что сила взаимодействия слабее ковалентной связи. Схема записи структуры выглядит следующим образом: Б ··· Нd+ – Аd-.
Только три химических элемента полностью проявляют донорские способности, и их атомы поставляют протоны для образования Н-связей: азот (N), кислород (O) и фтор (F). В атомах-акцепторах недостатка не наблюдается. Низкомолекулярным соединениям H-связь придаёт способность в обычных условиях иметь жидкое агрегатное состояние, как это происходит у этанола (C2H5OH), метанола (CH3OH) и воды (H2O), или становиться сжижающимися при охлаждении газами — аммиаком (NH3) и гидрофторидом (HF).
Проявление в неорганической химии
Определение «водородная связь» появилось в 1920 году. Его применили учёные Латимер и Родебуш для объяснения сущности аномалий, наблюдавшихся при кипении воды, предельных одноатомных спиртов и жидкого фтороводорода. При сопоставлении точек кипения в ряду водородсодержащих родственных соединений Н2O (вода), Н2S (сероводород), Н2Se (селеноводород) и Н2Te (теллуроводород) обнаружилось, что первый участник этого списка (H2O) переходит из жидкости в пар гораздо раньше, чем можно было бы ожидать, следуя закономерности, которой подчиняются остальные члены. Истинное значение точки кипения воды оказалось на 200° C выше ожидаемого.
Это справедливо и для другого ряда — NH3 (аммиак), PH3 (фосфин), H3As (арсин), Н3Sb (стибин), где фактическая (-33 °C) температура кипения аммиака на 80 градусов превышает ожидаемую. Если считать, что молекулы в жидкости удерживаются исключительно Ван-дер-Ваальсовыми силами, разрушающимися при переходе в газообразную фазу, то эти скачки не должны наблюдаться, а объяснить их невозможно.
Неожиданные повышения температур кипения привели к выводам о присутствии дополнительно связывающих молекулы сил, изменяющих физические свойства. Водородной связи принадлежит роль в создании аномальных температур кипения спиртов, если их сравнивать с аналогами без гидроксильных групп (-ОН). В перечне заслуг H-связей не только изменение точек кипения веществ, но и упрочнение их кристаллических решёток, вызывающее повышение температур плавления, поверхностного натяжения и вязкости.
Например, борная кислота с формулой H3BO3 имеет слоистую триклинную кристаллическую решётку, где каждая из молекул посредством H-связей крепится к трём другим. В результате образуются плоские слои, которые за счёт межмолекулярных связей создают кристаллическую структуру — «паркет» из шестиугольников.
При помощи инфракрасной спектроскопии сегодня можно достоверно выявить любой тип межмолекулярного взаимодействия: группы с Н-связями заметно отличаются по спектральным характеристикам от остальных случаев. Исследования структуры вещества помогают измерить дистанцию между водородом и атомом-акцептором, сравнить её с суммой радиусов и, если первое значение не превышает второе, доказать существование явления.
Понятие водных кластеров

Земля — чемпион по содержанию воды среди других планет Солнечной системы. Моря и океаны, реки и озёра, средние глубины которых достигают 6 тыс. метров, занимают 70% земной поверхности, а в областях полюсов сосредоточились огромные запасы влаги в виде снегов и льдов.
Трудно переоценить влияние воды на возникновение и существование жизни на нашей планете. Это связано с особенностями, нехарактерными для соединений, считающихся её близкими аналогами. Только вода находится в жидком и твёрдом состоянии при условиях, в которых водородные соединения серы или селена с большей атомной массой становятся газообразными.
Присутствие H-связей в молекулах воды обуславливает образование водных кластеров или комплексов, а димеры воды служат их простейшими примерами. Энергия их водородных связей ненамного больше энергии броуновского движения при нормальных условиях, но сильно отличается от мощности ковалентных связей в гидроксильных группах, а они в 200 раз превышают тепловые показатели. Вода из простой жидкости превращается в сложную, «связанную» сетью H-связей, хотя они относительно слабы и неустойчивы, самопроизвольно возникают и исчезают при температурных изменениях.
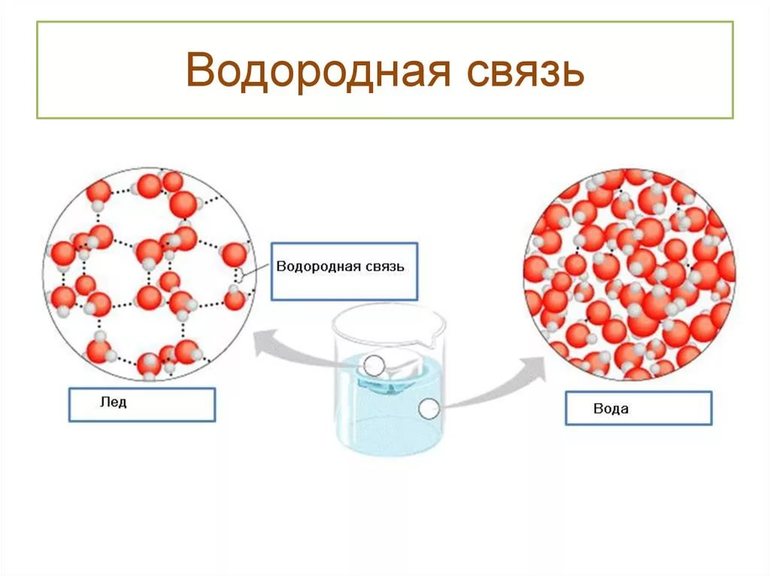
Кристаллическая структура льда имеет объёмную сетку из этих связей, и молекулы H2O расположены так, чтобы атомы водорода одних молекул оказывались направленными к атомам кислорода соседей. В ледяном кристалле между молекулами обязательно присутствуют пустоты, их объёмы немного превышают размеры отдельных молекул воды. Именно благодаря таким «карманам» плотность льда меньше, чем у его жидкой фазы, а гигантские айсберги остаются дрейфовать на поверхности, в то время как замерзание большинства других веществ существенно увеличивает их плотность.
Водородные связи сообщают воде уникальную характеристику, обеспечивающую существование разнообразных форм жизни в областях, где окружающие температуры опускаются ниже нуля. Если на минуту представить, что лёд начнёт тонуть в воде, то моря зимой рано или поздно промёрзнут до самого дна, и рыбы будут обречены на вымирание. Люди могли бы растапливать лёд для получения живительной влаги, но это потребует больших энергозатрат.

Ещё одно проявление H-связей — голубая окраска чистой воды в её толще. Колебание одной молекулы воды вызывает движение соседних частиц, соединенных с ней водородными связями. Красные лучи из состава солнечного спектра будут расходоваться на поддержание этих колебаний, поскольку больше всего соответствуют им энергетически. Происходит фильтрация красных лучей — их энергия поглощается и рассеивается в виде тепла колеблющимися молекулами.
Начинает проступать голубой участок спектра, уравновешивающий отсутствие красного. Вода самостоятельно окрасится в волшебный небесный цвет. Для этого необходимо, чтобы солнечные лучи прошли через двухметровую толщу чистой воды и потеряли достаточное количество красного спектра.
Значение для органических соединений
Многие органические вещества не могут растворяться в воде. Но если это происходит, то процесс не обходится без активного участия H-связей. Кислород и азот, главные доноры протонов, часто играют роли акцепторов. Органические соединения, содержащие O и N, легко растворяются в воде: здесь кислород и азот выступают в качестве атомов-акцепторов, а атомом-донором является кислород из молекул воды. Возникающие H-связи перемещают органическое вещество в раствор, «растаскивая» его на молекулы.

Просматривается эмпирическая закономерность: органическое соединение будет легко растворяться в воде, если в составе его молекул на каждый атом кислорода приходится не более 3 атомов углерода. Например, бензол C6H6 в воде растворяется плохо, но замена одной группы (-СН) на (-N) даёт пиридин С5Н5N, смешивающийся с водой в любых пропорциях.
Для неводных растворов, в которых растворителями служат органические вещества, тоже характерны H-связи. В них водород частично положительно поляризован, а поблизости обнаруживается молекула с сильным акцептором — чаще всего это бывает кислород. Жирные кислоты приобретают полезную способность растворяться в хлороформе HCCl3, а растворённый в ацетоне ацетилен получил важное техническое применение. Горючий газ C2H2 под давлением чувствителен к сотрясениям и взрывоопасен, но его растворение в ацетоне C3H6O позволяет безопасно хранить и транспортировать любые объёмы.
Трудно переоценить роль H-связей в прочных полимерных и биополимерных структурах. Целлюлоза (клетчатка древесины) в строении молекулы располагает гидроксильные группы по бокам полимерной структуры, в которой чередуются циклические фрагменты. Невысокая энергия единичной Н-связи, умноженная на количество по всей длине молекулярной цепи, вызывает в итоге мощное притяжение. Из-за этого целлюлозу можно растворить только в высокополярных растворителях — дигидроксотетрааммиакате меди, известном как реактив Швейцера.
Карбонильные (=C=O) и аминогруппы (-NH2) в расположенных рядом полимерных цепочках капрона и нейлона тоже образуют связи этого типа и увеличивают механическую прочность веществ, поскольку в полиамидных структурах создаются кристаллические фрагменты. Аналогично ведут себя полиуретаны и белки: витки белковых спиралей закрепляются всё теми же H-связями, возникающими при взаимодействии функциональных групп.

Полимерная макромолекула ДНК — хранилище запасов информации о живом организме, зашифрованной в чередующихся фрагментарных циклах. Их карбонильные и аминогруппы имеют четыре типа азотистых оснований (аденин A, гуанин G, тимин T, цитозин C) и располагаются в форме боковых ответвлений по длине молекулы. От порядка их чередования зависят индивидуальные особенности всего живого на планете. Взаимодействия пар в составе аминогруппы и атома азота дают начало множеству Н-связей, которые удерживают 2 молекулы ДНК в виде классической двойной спирали.
Водородная связь

Водородная связь — форма ассоциации между электроотрицательным атомом и атомом водорода H, связанным ковалентно с другим электроотрицательным атомом. В качестве электроотрицательных атомов могут выступать N, O или F. Водородные связи могут быть межмолекулярными или внутримолекулярными. [1]
Содержание
Природа
Часто водородную связь рассматривают как электростатическое взаимодействие, усиленное небольшим размером водорода, которое разрешает близость взаимодействующих диполей. Тогда об этом говорят как о разновидности донорно-акцепторной связи, невалентном взаимодействии между атомом водорода H, ковалентно связанным с атомом A группы A-H молекулы RA-H и электроотрицательным атомом B другой молекулы (или функциональной группы той же молекулы) BR’. Результатом таких взаимодействий являются комплексы RA-H•••BR’ различной степени стабильности, в которых атом водорода выступает в роли «моста», связывающего фрагменты RA и BR’.
Особенностями водородной связи, по которым её выделяют в отдельный вид, является её не очень высокая прочность [2] , её распространенность и важность, особенно в органических соединениях [3] , а также некоторые побочные эффекты, связанные с малыми размерами и отсутствием дополнительных электронов у водорода.
В настоящее время в рамках теории молекулярных орбиталей водородная связь рассматривается как частный случай ковалентной с делокализацией электронной плотности по цепи атомов и образованием трёхцентровых четырёхэлектронных связей (например, -H•••[F-H•••F]-).
История
В книге The Nature of Chemical Bond and the Structure of Molecules and Crystals Лайнуса Полинга, впервые изданной в 1939 году, первое упоминание водородной связи приписывается Муру и Винмиллу. Они использовали водородную связь, чтобы обосновать факт, что у гидроокиси триметиламмония более слабая основа, чем у гидроксида тетраметиламмония. [4] Описание водородных связей в воде было сделано в 1920 году Латимером и Родебушем [5] .
Свойства
Энергия водородной связи значительно меньше энергии обычной ковалентной связи (не превышает 40 кДж/моль). Однако этой энергии достаточно, чтобы вызвать ассоциацию молекул, то есть их объединение в димеры или полимеры. Именно ассоциация молекул служит причиной аномально высоких температур плавления и кипения таких веществ, как фтороводород, вода, аммиак.
Связь этого типа, хотя и слабее ионной и ковалентной связей, тем не менее играет очень важную роль во внутри- и межмолекулярных взаимодействиях. Водородные связи во многом обусловливают физические свойства воды и многих органических жидкостей (спирты, карбоновые кислоты, амиды карбоновых кислот, сложные эфиры).
Прочность водородной связи (энтальпия образования комплекса) зависит от полярности комплекса и колеблется от ~ 6 кДж/моль для комплексов молекул галогеноводородов с инертными газами до 160 кДж/моль для ион-молекулярных комплексов (AHB) ± ; так, для комплекса (H2O•H•OH2) + образованного H2O и H3O + — 132 кДж/моль в газовой фазе.
В воде
Механизм Гротгуса
Аномально высокая теплоёмкость воды, а также теплопроводность многоатомных спиртов обеспечивается многочисленными водородными связями. Одна молекула воды может образовать до четырёх классических водородных связей с соседями (с учётом бифуркатных Н-связей до 5-6).
Водородные связи повышают температуру кипения, вязкость и поверхностное натяжение жидкостей. Водородные связи ответственны за многие другие уникальные свойства воды.
Водные кластеры

Водородная связь между молекулами воды обозначена чёрными линиями. Жёлтые линии обозначают ковалентную связь, которая удерживает вместе атомы кислорода (красный) и водорода (серый).
Согласно современным представлениям, наличие водородных связей между молекулами воды приводит к возникновению так называемых водных кластеров или комплексов. Простейшим примером такого кластера может служить димер воды:

= mathsf cdots mathsf” width=”” height=”” />

Энергия водородной связи в димере воды составляет 0,2 эВ (≈ 5 ккал/моль), что всего на порядок больше, чем характерная энергия теплового движения при температуре 300 К. В то же время энергия ковалентной O-H связи в 200 раз больше тепловой энергии. Таким образом, водородные связи относительно слабы и неустойчивы: предполагается, что они могут легко возникать и исчезать в результате тепловых флуктуаций. Это, в частности, приводит к тому, что вода должна рассматриваться не как «простая», а как «связанная жидкость»: вода представляется как сеть молекул ” width=”” height=”” />, соединённых водородными связями [6] .
В нуклеиновых кислотах и белках
Водородная связь в значительной мере определяет свойства и таких биологически важных веществ, как белки и нуклеиновые кислоты. В частности, элементы вторичной структуры (например, α-спирали, β-складки) и третичной структуры в молекулах белков, РНК и ДНК стабилизированы водородными связями. В этих макромолекулах, водородные связи сцепляют части той же самой макромолекулы, заставляя её сворачиваться в определенную форму. Например, двойная спиральная структура ДНК, определяется в значительной степени наличием водородных связей, сцепляющих пары нуклеотидов, которые связывают одну комплементарную нить с другой.
В полимерах
Много полимеров усилены водородными связями в их главных цепях. Среди синтетических полимеров самый известный пример — нейлон, где водородные связи играют главную роль в кристаллизации материала. Водородные связи также важны в структуре полученных искусственно полимеров (например, целлюлозы) и в многих различных формах в природе, таких как древесина, хлопок и лён.





